Última actualización: marzo 2026
La próstata crece con la edad. Es algo tan inevitable como las canas. A partir de los 30 años, el tejido prostático comienza a desarrollar lo que llamamos hiperplasia benigna de próstata (HBP), un crecimiento que, en muchos hombres, acabará produciendo síntomas molestos o complicaciones que afectan seriamente a la calidad de vida.
Si usted está leyendo este artículo, probablemente ya le han diagnosticado un problema de próstata y está buscando información sobre las opciones quirúrgicas. Le voy a explicar con claridad qué es el HoLEP, por qué lo considero el mejor tratamiento quirúrgico disponible para la HBP, y qué hemos aportado en ICUA para perfeccionar esta técnica a lo largo de más de 20 años.
¿Cuándo la próstata se convierte en un problema?
Los síntomas aparecen cuando el crecimiento prostático comprime la uretra y dificulta la salida de la orina. El paciente nota que el chorro es débil, que tarda en comenzar a orinar, que tiene la sensación de no vaciar la vejiga completamente, que se levanta varias veces por la noche. En casos más avanzados, aparecen complicaciones serias: retención urinaria aguda (no poder orinar en absoluto y necesitar una sonda), infecciones urinarias repetitivas, sangrado prostático, cálculos en la vejiga e incluso daño renal.
Suelo decir que hay dos tipos de pacientes: los que tienen obligación quirúrgica — retención, cálculos, insuficiencia renal, sangrado, infecciones de repetición — y los que no están obligados a operarse pero cumplen criterios para que se lo recomendemos. En ambos casos, es importante saber que la HBP es una enfermedad progresiva. La vejiga se deteriora si la obstrucción no se trata adecuadamente, y existe una ventana de oportunidad para actuar antes de que el daño vesical sea irreversible.
¿Qué es el HoLEP?
HoLEP son las siglas de Holmium Laser Enucleation of the Prostate — enucleación de la próstata con láser de holmio. Es una técnica quirúrgica que utiliza un láser de alta precisión para separar el adenoma prostático (el tejido que ha crecido y obstruye) de la cápsula de la próstata, y extraerlo completamente.
La técnica fue desarrollada inicialmente en Nueva Zelanda en los años 90 por los doctores Gilling y Fraundorfer. Desde entonces, ha experimentado una evolución enorme, con múltiples refinamientos técnicos que han mejorado sus resultados y facilitado su aprendizaje. Las guías clínicas de la Asociación Europea de Urología (EAU) y de la Asociación Americana de Urología (AUA) la recomiendan como una opción estándar, independiente del tamaño de la próstata.
¿En qué se diferencia el HoLEP de otras técnicas?
Existen muchas opciones para operar la próstata, y es normal que los pacientes se sientan confusos. La diferencia fundamental está en el concepto: enuclear no es lo mismo que resecar ni que vaporizar.
La resección transuretral (RTU) es la técnica clásica. Un asa eléctrica va cortando el adenoma en fragmentos pequeños, como si tallara una estatua desde dentro. El problema es que nunca se extrae todo el tejido — siempre quedan restos que pueden volver a crecer. Y en próstatas grandes, el procedimiento se alarga mucho, aumentando el riesgo de sangrado y otras complicaciones. La tasa de reintervención a largo plazo con RTU se sitúa entre el 10 y el 15%.
La vaporización con láser verde (GreenLight) destruye el tejido prostático evaporándolo. Es muy segura en cuanto a sangrado, pero tiene una limitación: el tejido desaparece, no queda muestra para analizar en el laboratorio, y en próstatas grandes la intervención es muy lenta y a menudo incompleta.
La enucleación (HoLEP) sigue el plano anatómico natural entre el adenoma y la cápsula, separándolos completamente. Es el mismo principio que la cirugía abierta clásica — que durante décadas fue el tratamiento de referencia para próstatas grandes — pero sin incisiones, sin transfusiones y con una recuperación mucho más rápida. Y lo fundamental: se extrae todo el adenoma, por lo que la tasa de retratamiento es inferior al 2%.
La diferencia conceptual es esta: la RTU y la vaporización trabajan desde la uretra hacia fuera, abriendo un canal a través del adenoma. El HoLEP trabaja desde fuera hacia dentro, despegando todo el adenoma de la cápsula. Es una cirugía anatómica, completa y definitiva.
¿Qué es la enucleación en bloque?
La técnica original de HoLEP separaba el adenoma en dos o tres lóbulos que se iban volcando por separado a la vejiga. Era eficaz, pero técnicamente difícil y con una curva de aprendizaje larga.
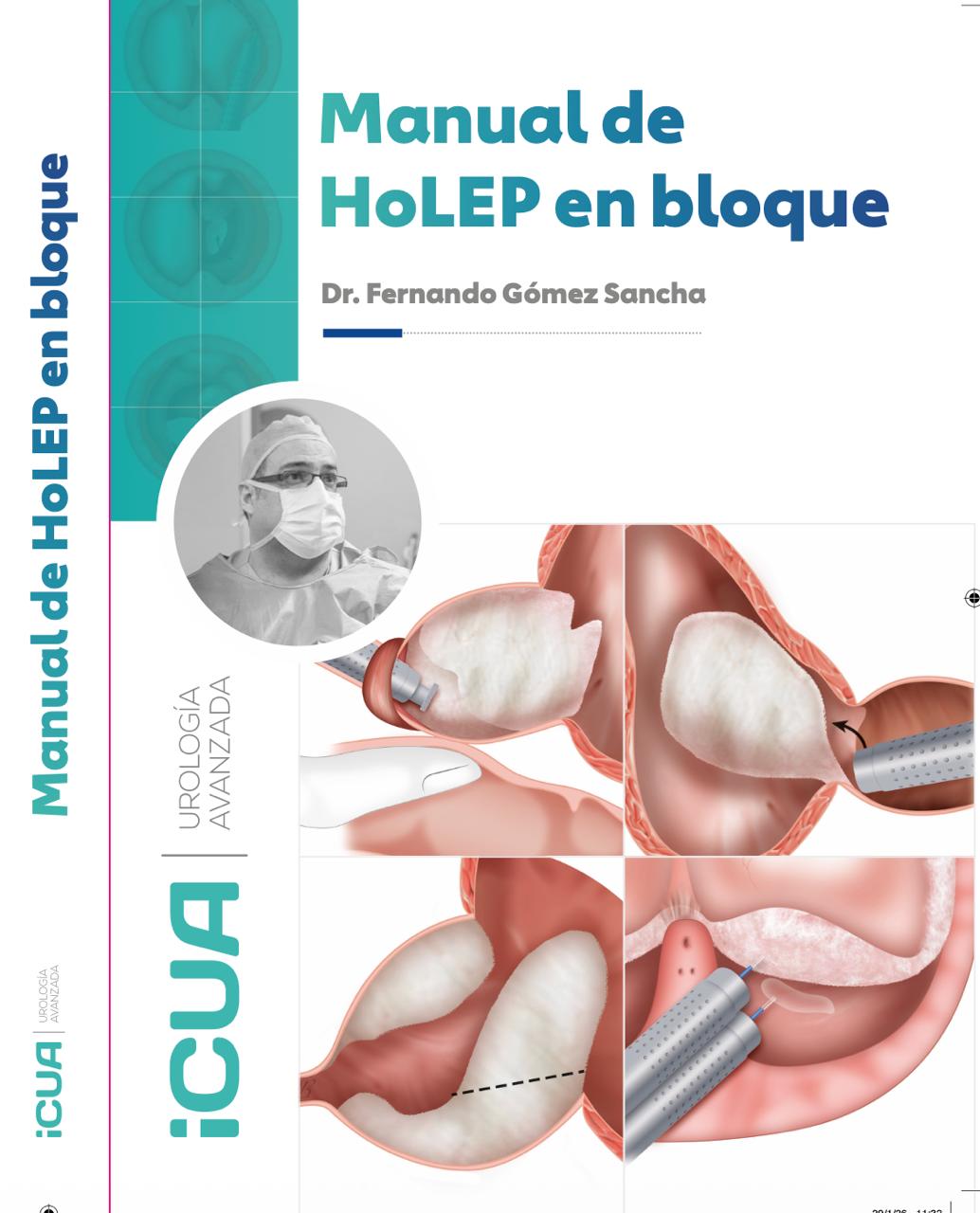
A lo largo de mi experiencia, primero con el láser verde y posteriormente con el láser de holmio, desarrollé una técnica que llamamos enucleación en bloque con liberación apical precoz y preservación de la mucosa esfinteriana. En lugar de dividir el adenoma en fragmentos, lo despegamos de la cápsula en una sola pieza — en bloque, como se pela una naranja entera.
La intervención comienza marcando el límite entre el ápex del adenoma y el esfínter urinario externo — lo que llamamos la "línea blanca". Desde ahí, liberamos precozmente el esfínter del adenoma, protegiéndolo desde el primer momento de la cirugía. A continuación, vamos despegando el adenoma circunferencialmente hasta volcarlo entero a la vejiga, donde se fragmenta con un instrumento llamado morcelador para poder extraerlo.
Esta técnica tiene varias ventajas demostradas:
Es más rápida. Un ensayo aleatorizado publicado en 2025 comparó directamente la enucleación en bloque con la técnica clásica por lóbulos. La técnica en bloque redujo el tiempo de enucleación de 74 a 62 minutos y el tiempo operatorio total de 95 a 79 minutos, con menor consumo de energía láser. Un estudio prospectivo de 600 pacientes también confirmó que la técnica de tres lóbulos es significativamente más lenta que la técnica en bloque.
Protege mejor la continencia. La liberación precoz del esfínter minimiza la tracción sobre él durante toda la cirugía. En nuestra serie de 754 pacientes consecutivos operados con esta técnica, publicada en World Journal of Urology en 2025, la tasa de incontinencia de esfuerzo a los 6 meses fue del 0,15% para próstatas menores de 120 gramos y del 0,9% para las mayores. Son cifras extraordinariamente bajas.
Es más fácil de aprender. Un estudio publicado en Translational Andrology and Urology demostró que con la técnica en bloque, un cirujano principiante alcanza un nivel razonable de competencia en 20-30 casos, frente a los 50 que se necesitan con la técnica clásica de tres lóbulos. Un estudio de la Universidad de Mannheim con 500 casos consecutivos en bloque confirmó una mejora continua en eficiencia incluso después de cientos de procedimientos.
Funciona igual de bien en próstatas de cualquier tamaño. De hecho, cuanto más grande es la próstata, más eficiente es la enucleación en bloque. En nuestra serie publicada, la eficiencia de enucleación en próstatas grandes fue de 3,1 gramos por minuto — el doble que en próstatas más pequeñas. Hemos operado próstatas de 300, 400 y hasta 500 gramos con esta técnica, con resultados excelentes.
¿Para quién está indicado el HoLEP?
Una de las grandes ventajas del HoLEP es que no tiene límite de tamaño prostático. Mientras que la RTU tiene un límite práctico en torno a 80 gramos y otros tratamientos como Aquablation tienen un rango limitado, el HoLEP puede tratar próstatas de cualquier volumen. Es la única técnica endoscópica que sustituye verdaderamente a la cirugía abierta, con la misma eficacia pero sin sus inconvenientes.
Está especialmente indicado en:
- Próstatas de gran tamaño (más de 80-100 gramos), donde otras técnicas endoscópicas se quedan cortas.
- Pacientes anticoagulados, gracias a la excelente capacidad hemostática del láser de holmio. La tasa de transfusión en nuestra serie es inferior al 1%.
- Pacientes portadores de sonda permanente, que necesitan una solución definitiva a su obstrucción.
- Pacientes con cálculos vesicales, que pueden tratarse en la misma intervención con el mismo láser.
- Cualquier paciente que busque una solución definitiva con la menor tasa de retratamiento posible.
La importancia de la experiencia del cirujano
Debo ser honesto en un punto: el HoLEP es una técnica que depende mucho de la habilidad y la experiencia del cirujano. No basta con tener el láser — hay que saber usarlo. La curva de aprendizaje existe, aunque las técnicas modernas como la enucleación en bloque la han acortado significativamente.
¿Cómo saber si su cirujano tiene la experiencia necesaria? Hay algunas preguntas razonables que puede hacer: cuántas enucleaciones ha realizado, si tiene resultados propios publicados, si forma a otros cirujanos en la técnica. Un cirujano que enseña a otros tiene, por definición, un dominio profundo de lo que hace.
En ICUA llevamos realizando prostatectomías con láser desde 2003 y enucleaciones desde 2007. Acumulamos más de 10.000 enucleaciones prostáticas. He descrito la técnica de enucleación en bloque con láser verde (GreenLEP) publicada en World Journal of Urology en 2015, y la técnica de HoLEP en bloque con liberación apical precoz publicada en 2019. Nuestra serie de 754 casos consecutivos con esta técnica fue publicada en 2025. Participamos como coautores en el registro REAP, la mayor base de datos multicéntrica mundial de enucleación prostática, con 6.193 pacientes de 10 centros en 7 países. Hemos formado a cirujanos de más de 60 países en nuestros quirófanos de Madrid y Sofía.
¿Qué puede esperar tras un HoLEP?
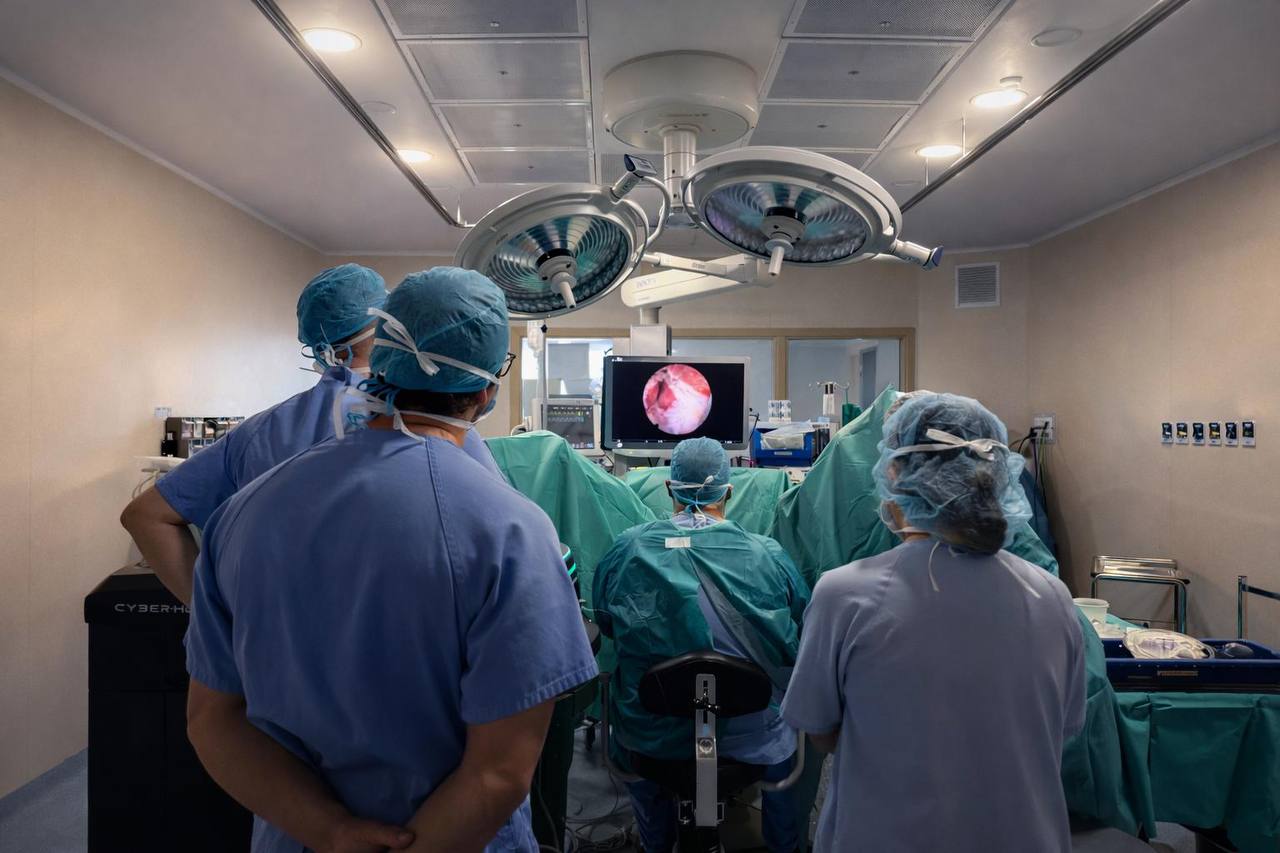
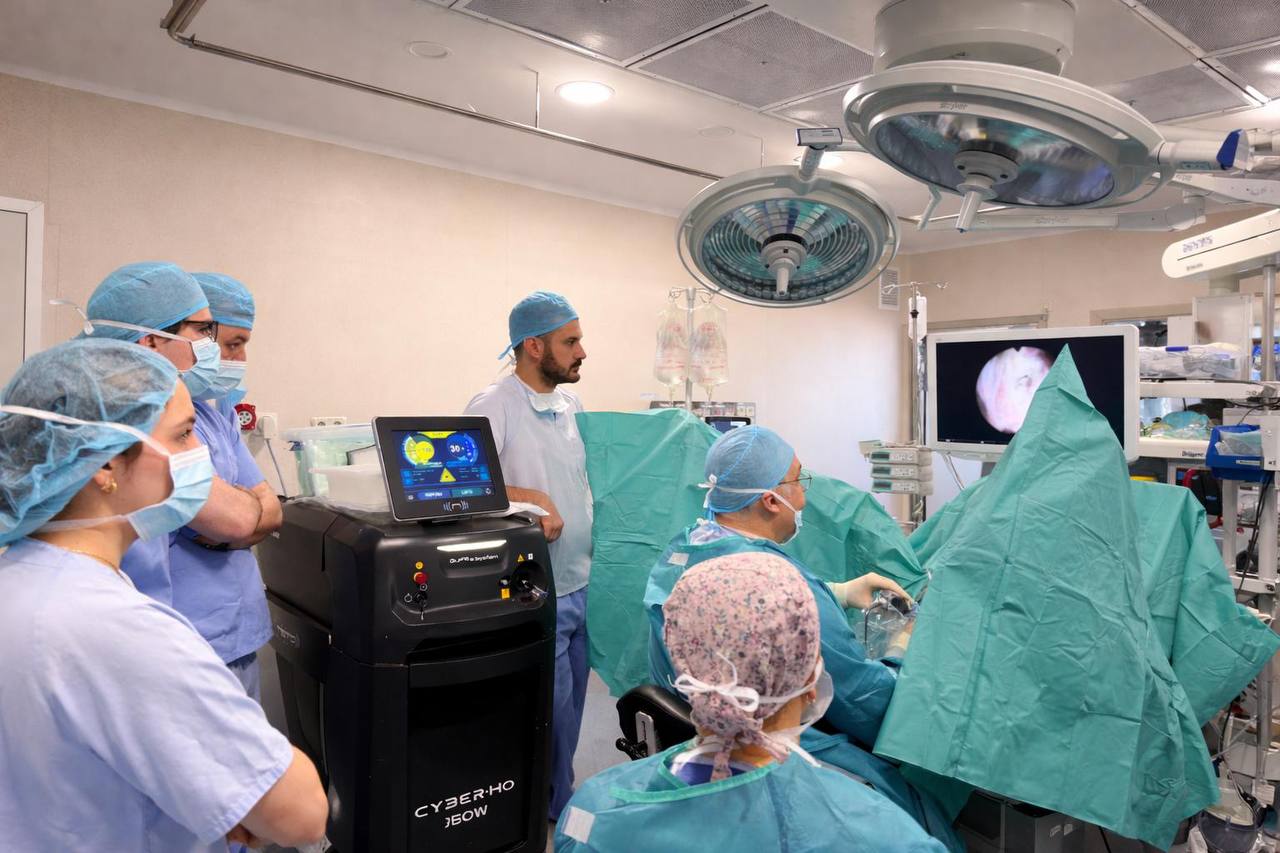
La mayoría de los pacientes ingresan por la mañana, se operan con anestesia raquídea (de cintura para abajo) y pueden irse a casa al día siguiente, sin sonda en la mayoría de los casos. El flujo urinario mejora de forma inmediata y drástica — en nuestra serie, el flujo máximo pasa de 8 ml/s antes de la cirugía a 24-28 ml/s después.
La recuperación es rápida: vida normal en 2-3 días, aunque durante las primeras semanas pueden persistir algunas molestias urinarias como urgencia o escozor, que son transitorias y van desapareciendo progresivamente.
Tras el HoLEP, el PSA debe quedar por debajo de 1 ng/mL — un dato importante para el seguimiento posterior que refleja la radicalidad de la enucleación. En nuestra serie, la reducción del PSA fue del 93-94%.
La inmensa mayoría de los pacientes dejan de necesitar toda la medicación prostática que estaban tomando y no vuelven a necesitar cirugía.
Solicite una consulta en ICUA · Clínica CEMTRO, Madrid — o una videoconsulta si está fuera de España.
📞 +34 91 435 28 44 · ✉ icua@icua.es
Porque al final, como les digo a mis pacientes: no hay que ser el primero en operarse, pero tampoco el último.
Referencias científicas
- Saitta G, Becerra JEA, Del Álamo JF, et al. 'En Bloc' HoLEP with early apical release in men with benign prostatic hyperplasia. World J Urol. 2019;37:2451-2458. PubMed
- Iscaife A, Rodríguez Socarrás M, Talizin TB, et al. Contemporary results of En Bloc HoLEP for large prostates. World J Urol. 2025;43:401. PubMed
- Gomez Sancha F, Rivera VC, Georgiev G, et al. Common trend: move to enucleation — Is there a case for GreenLight enucleation? Development and description of the technique. World J Urol. 2015;33:539-547. DOI (Open Access)
- Gauhar V, Gómez Sancha F, Enikeev D, et al. Results from a global multicenter registry of 6193 patients to refine endoscopic anatomical enucleation of the prostate (REAP). World J Urol. 2023;41:3033-3040. PubMed
- Gauhar V, Lim EJ, Fong KY, et al. Influence of early apical release on outcomes in endoscopic enucleation of the prostate: results from a multicenter series of 4392 patients. Urology. 2024;187:154-161. DOI
- Rücker F, Lehrich K, Böhme A, et al. A call for HoLEP: en-bloc vs. two-lobe vs. three-lobe. World J Urol. 2021;39:2337-2345. DOI
- Wenk MJ, Hartung FO, Egen L, et al. The long-term learning curve of HoLEP in the en-bloc technique: a single surgeon series of 500 consecutive cases. World J Urol. 2024;42:436. PubMed
- Li P, Wang C, Tang M, et al. The en bloc method is feasible for beginners learning to perform HoLEP. Transl Androl Urol. 2023;12(3):379-390. PubMed Central